Instrucción
de uso solución estéril para irrigación intravesical a base de ácido hialurónico
INSTYLAN
Descripción:
INSTYLAN es una solución viscosa estéril, transparente e incolora a base de ácido hialurónico de origen no animal con Ph fisiológico.
INSTYLAN es un agente protector viscoelástico de la sustancia intercelular de la vejiga y la uretra.
Clasificación del producto:
Dispositivo médico – esterilizado por vapor – libre de pirógenos – Clase IIa.
Empaquetado:
Bolsa de plástico desechable precargada de 50 ml que contiene 0,16% (80 mg/ 50 ml) de hialuronato sódico.
Cada caja contiene:
– 1 Bolsa de polímero con boquilla para la sonda urinaria en una caja de cartón.
Composición de calidad:
50 ml de solución estéril para irrigación intravesical a base de ácido hialurónico INSTYLAN 0,16% contiene:
- Hialuronato de sodio
Excipientes: Cloruro de sodio, Agua para inyección, Tampón fosfato
Indicaciones:
- Deficiencia de una capa de glicosaminoglicanos (GAG) y restablecimiento de la capa protectora de lamucosa de la vejiga tras intervenciones invasivas (como la cistoscopia, la resección transuretral (RTU) de lapróstata, la ureteroscopia, etc.).
- Cistitis bacteriana recurrente.
- Cistitis intersticial.
- Síndrome de vejiga dolorosa.
- Cistitis hemorrágica.
- Cistitis actínica.
- Cistitis inducida por la quimioterapia
Modo de acción:
El ácido hialurónico está presente en todos los tejidos y es el componente más importante de la matriz intercelular, por lo que constituye una parte significativa de los glucosaminoglicanos del urotelio de la vejiga y la uretra.
Cuando se inyecta en la cavidad de la vejiga, crea una capa viscoelástica protectora de tipo natural en la superficie del urotelio, protegiendo así la mucosa de la vejiga de factores irritantes y perjudiciales.
Contraindicaciones:
- No utilizar el producto en pacientes con hipersensibilidad al ácido hialurónico o con anteced entes de reacciónalérgica a alguno de los componentes de la solución.
- No utilizar el producto durante el embarazo y la lactancia.
- No utilizar el producto en niños y adolescentes menores de 18 años.
Método de aplicación:
INSTYLAN está destinado únicamente a la instilación en la vejiga. Este procedimiento debe ser realizado por un especialista con la experiencia y formación médica adecuadas para cumplir con todas las normas del sondaje urinario.
INSTYLAN está destinado a la administración intravesical, una vez por semana. El curso es de 4 a 12 instilaciones.
Antes de la administración de INSTYLAN, la vejiga debe estar vacía.
INSTYLAN se inyecta en la cavidad vesical mediante una sonda urinaria. Siga cuidadosamente las operaciones sugeridas por el protocolo normal para el manejo del catéter vesical. Tras la administración de la solución, se retira la sonda.
El tiempo de retención recomendado de la solución en la luz de la vejiga es de 30 minutos a 2 horas. A continuación, la vejiga debe vaciarse fisiológicamente.
Antes de su uso, la bolsa con la solución debe calentarse a la temperatura corporal.
La solución calentada a la temperatura corporal reduce las molestias del paciente. Este procedimiento sólo debe realizarse con calor seco (por ejemplo, almohadilla térmica o placa caliente).
Las soluciones no deben calentarse en agua debido al mayor riesgo de contaminación. Para evitar posibles daños a la bolsa de polímero y daños o molestias al paciente, las soluciones no deben calentarse en el microondas.
Deben seguirse estrictas normas de asepsia durante todo el procedimiento.
Cómo utilizarlo:
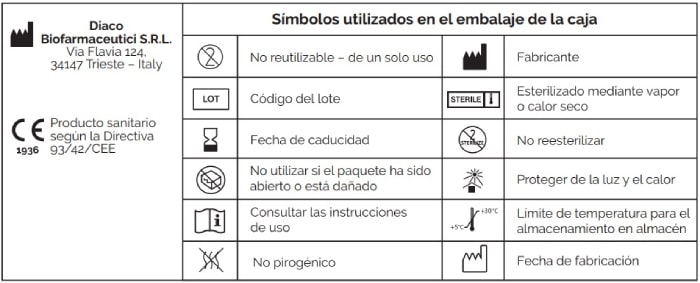
- Verificar la integridad del embalaje externo, la fecha de caducidad, el volumen del dispositivo
- Abrir la bolsa de plástico para sacar el dispositivo de plástico
- Controlar la integridad del dispositivo de plástico
- Leer las instrucciones de uso
- Retirar el tapón naranja del cierre luer del dispositivo de plástico
- Introducir el luer-lock en el catéter urinario
- Romper el cono rojo interno del luer-lock para liberar la solución en el catéter urológico
- Empuja el dispositivo de plástico para permitir la salida de todo el volumen de solución
- Realiza el procedimiento y comprueba continuamente de forma visual
Reacciones adversas:
Reacciones de hipersensibilidad. En casos raros: irritación de la vejiga, calambres en la vejiga, disuria, dolor, diarrea, mareos. En caso de cualquier reacción adversa, debe interrumpir inmediatamente el uso del producto sanitario e informar al médico y al fabricante.
Advertencias:
- El producto no debe administrarse por vía oral
- No utilizar si la solución no es transparente e incolora
- El producto debe utilizarse inmediatamente después de abrirlo
- El producto está destinado a un solo uso
- No reesterilizar. La esterilización repetida puede causar contaminación cruzada
- No utilizar si el envase ha sido abierto o está dañado
- No utilizar después de la fecha de caducidad
Conservación:
2 años en un envase intacto.
Condiciones de almacenaje:
Almacenar a una temperatura entre +5 ° y 30 °C inclusive, protegido de la luz. No congelar. Mantener fuera del alcance de los niños.
Eliminación:
Elimine los materiales utilizados de acuerdo con la legislación vigente sobre los requisitos de eliminación de residuos médicos.
Última revision: 12/2020
Antes de la aplicación de los productos de este medio informativo, se recomienda consultar a su médico y leer la instrucción.
Información sobre el producto de la destinación médica para la actividad profesional de los especialistas de la Salud. INSTYLAN (INSTYLAN) 0,16% gel viscoso, sin color de ácido hialurónico, no de orígen animal, estéril con PH fisiológico.
INSTYLAN 0,16% está aprobado como producto de la destinación médica de la ІІa clase. Certificado de aceptabilidad de UE. Número de registro: DD 60107286 0001. Productor: Diaco Biofarmaceutici S.R.L. Via Flavia 124, 34147, Trieste, Italy. E-mail: info@diaco.it. www.diaco.it.