Istruzioni per l`uso
di dispositivo medico
Soluzione sterile a base di acido ialuronico per irrigazione intravescicale
INSTYLAN
Descrizione
INSTYLAN è una soluzione sterile, trasparente, incolore e viscosa a base di acido ialuronico di origine non animale a Ph fisiologico.
INSTYLAN è un agente viscoelastico che protegge la sostanza intercellulare di vescica e uretra.
Classificazione del prodotto
Dispositivo medico – sterilizzato a vapore – apirogeno – Classe IIa.
Confezione
Sacca in plastica monouso preriempita da 50 ml contenente una soluzione di ialuronato sodico allo 0,16% (80 mg/ 50 ml).
Ogni confezione contiene
– 1 Sacca in polimero con un beccuccio per catetere urinario in scatola di cartone.
Composizione qualitativa
50 ml di soluzione sterile a base di acido ialuronico per irrigazione intravescicale INSTYLAN 0,16% contengono:
- Sodio ialuronato
Eccipienti: cloruro di sodio, acqua per preparazioni iniettabili, tampone fosfato.
Indicazioni
- Carenza dello strato di glicosamminoglicani (GAG) e ripristino dello strato protettivo della mucosa vescicale dopo interventi invasivi (quali cistoscopia, resezione transuretrale (TUR) della prostata, ureteroscopia, ecc.).
- Cistite batterica ricorrente.
- Cistite interstiziale.
- Sindrome dolorosa della vescica.
- Cistite emorragica.
- Cistite attinica.
- Cistite indotta da chemioterapia.
Meccanismo di azione
L’acido ialuronico è contenuto in tutti i tessuti e rappresenta il componente più importante della matrice intercellulare, costituendo pertanto una parte significativa dei glicosamminoglicani dell’urotelio di vescica e uretra.
Quando viene iniettato nella cavità vescicale, l’acido ialuronico crea sulla superficie dell’urotelio uno strato protettivo visco-elastico simile a quello naturale, proteggendo di tal modo la mucosa vescicale da fattori irritanti e danneggianti.
Controindicazioni
- Non utilizzare il prodotto su pazienti con ipersensibilità all’acido ialuronico o pazienti con anamnesi di reazione allergica a qualsiasi dei componenti della soluzione.
- Non utilizzare il prodotto su pazienti in gravidanza o che stanno allattando.
- Non utilizzare il prodotto su bambini e adolescenti di età inferiore a 18 anni
Metodo di applicazione
INSTYLAN è destinato esclusivamente all’instillazione vescicale. Tale procedura deve essere eseguita da uno specialista con esperienza e formazione medica che soddisfano tutti gli standard richiesti per la cateterizzazione urinaria.
INSTYLAN è destinato alla somministrazione intravescicale, una volta alla settimana. Il ciclo prevede da 4 a 12 instillazioni.
Prima della somministrazione di INSTYLAN, la vescica deve essere svuotata.
INSTYLAN è iniettato nella cavità vescicale mediante un catetere urinario. Seguire attentamente le operazioni suggerite dal normale protocollo per la gestione del catetere vescicale. Dopo la somministrazione della soluzione il catetere viene rimosso.
Il tempo raccomandato di ritenzione della soluzione nel lume vescicale è compreso tra 30 minuti e 2 ore. Successivamente la vescica deve essere svuotata fisiologicamente.
Prima dell’uso, la sacca contenente la soluzione deve essere riscaldata alla temperatura corporea.
Il riscaldamento della soluzione alla temperatura corporea riduce il fastidio per il paziente. Tale procedura deve essere eseguita esclusivamente mediante l’uso di calore secco (ad esempio mediante riscaldamento con cuscino o piastra riscaldanti).
Le soluzioni non devono essere riscaldate in acqua a causa dell’aumento del rischio di contaminazione. Al fine di evitare potenziali danni alla sacca in polimero e lesioni o fastidio al paziente, le soluzioni non devono essere riscaldate in un forno a microonde.
Seguire rigorosamente le regole di asepsi durante l’intera procedura.
Come usare il dispositivo
- Verificare l’integrità della confezione esterna, la data di scadenza e il volume del dispositivo
- Aprire il sacchetto di plastica ed estrarre il dispositivo in plastica
- Controllare l’integrità del dispositivo in plastica
- Leggere le istruzioni per l’uso
- Rimuovere il tappo arancione dal luer-lock del dispositivo in plastica
- Inserire il luer-lock nel catetere urinario
- Spezzare il cono rosso interno del luer-lock per rilasciare la soluzione nel catetere urologico
- Premere il dispositivo in plastica per consentire la fuoriuscita dell’intero volume di soluzione
- Eseguire la procedura sotto controllo visivo continuo
Reazioni avverse
Reazioni di ipersensibilità. In casi rari: irritazione della vescica, crampi vescicali, disuria, dolore, diarrea, capogiro. In caso di reazioni avverse, interrompere immediatamente l’uso del dispositivo medico e informare il medico e il produttore.
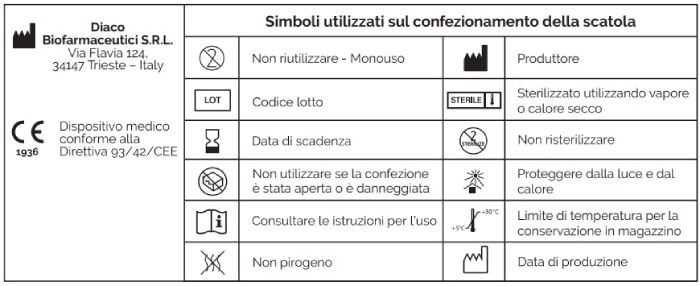
Avvertenze
- Il prodotto non deve essere somministrato per via orale
- Non utilizzare se la soluzione non è trasparente e incolore
- Il prodotto deve essere utilizzato immediatamente dopo l’apertura
- Il prodotto è esclusivamente monouso
- Non risterilizzare. La ripetizione della sterilizzazione può causare cross-contaminazione
- Non utilizzare se la confezione è stata aperta o è danneggiata
- Non utilizzare dopo la data di scadenza
Durata di conservazione
2 anni nella confezione intatta.
Condizioni di conservazione
Conservare a una temperatura compresa tra +5 ° e 30 °C inclusi, al riparo dalla luce. Non congelare. Conservare fuori dalla portata dei bambini.
Smaltimento
Smaltire i materiali utilizzati conformemente alle leggi applicabili relative agli obblighi per lo smaltimento dei rifiuti sanitari.
Edizione: 12/2020
Prima di usare i dispositivi medici che vengono proposti da questo sito si consiglia di consultare il proprio medico e leggere attentamente anche le istruzioni per l'uso.
Informazione sui dispositivi medici per il attività professionale degli operatori sanitari. INSTYLAN (INSTILAN) 0,16% incolore, trasparente, gel viscoso di acido ialuronico di origine non animale, sterile, pH fisiologico.
INSTYLAN 0,16% approvato come dispositivo medico della classe ІІa. Dichiarazione di conformità UE. Numero di registrazione: DD 60107286 0001.
Produttore: Diaco Biofarmaceutici S.R.L. Via Flavia 124, 34147, Trieste, Italia. E-mail: info@diaco.it. www.diaco.it.